MASA ATÓMICA
La masa atómica es considerada como la masa total de protones y neutrones en un solo átomo (cuando el átomo no tiene movimiento). La masa atómica es algunas veces usada incorrectamente como un sinónimo de masa atómica relativa, masa atómica media y peso atómico; estos últimos difieren sutilmente de la masa atómica. La masa atómica está definida como la masa de un átomo, que sólo puede ser de un isotopo a la vez, y no es un promedio ponderado en las abundancias de los isotopos En el caso de muchos elementos que tienen un isotopo dominante, la similitud/diferencia numérica real entre la masa atómica del isótopo más común y la masa atómica relativa o peso atómico estándar puede ser muy pequeña, tal que no afecta muchos cálculos bastos, pero tal error puede ser crítico cuando se consideran átomos individuales. Para elementos con más de un isótopo común, la diferencia puede llegar a ser de media unidad o más (por ejemplo, cloro). La masa atómica de un isótopo raro puede diferir de la masa atómica relativa o peso atómico estándar en varias unidades de masa.
PESO ATÓMICO
El peso atómico estándar se refiere a la media de las masas atómicas relativas de un elemento en el medio local de la corteza terrestre y la atmósfera terrestre, como está determinado por la Commission on Atomic Weights and Isotopic Abundances (Comisión de Pesos Atómicos y Abundancias Isotópicas) de la IUPAC. Estos valores son los que están incluidos en una tabla periódica estándar, y es lo que es más usado para los cálculos ordinarios. Se incluye una incertidumbre en paréntesis que frecuentemente refleja la variabilidad natural en la distribución isotópica, en vez de la incertidumbre en la medida. Para los elementos sintéticos, el isótopo formado depende de los medios de síntesis, por lo que el concepto de abundancia isotópica natural no tiene sentido. En consecuencia, para elementos sintéticos, el conteo total de nucleones del isótopo más estable (esto es, el isótopo con la vida media más larga) está listado en paréntesis en el lugar del peso atómico estándar. El litio representa un caso único, donde la abundancia natural de los isótopos ha sido perturbada por las actividades humanas al punto de afectar la incertidumbre en su peso atómico estándar, incluso en muestras obtenidas de fuentes naturales, como los ríos.
MASA ATÓMICA RELATIVA
La masa atómica relativa es un sinónimo para peso atómico y está cercanamente relacionado a masa atómica promedio (pero no es un sinónimo de masa atómica), la media ponderada de las masas atómicas de todos los átomos de un elemento químico encontrados en una muestra particular, ponderados por abundancia isotópica.3 Esto es usado frecuentemente como sinónimo para peso atómico relativo, y no es incorrecto hacer así, dado que los pesos atómicos estándar son masas atómicas relativas, aunque es menos específico. La masa atómica relativa también se refiere a ambientes no terrestres y ambientes terrestres altamente específicos que se desvían de la media o tienen diferentes certidumbres (número de cifras significativas) que los pesos atómicos estándar.
La masa isotópica relativa es la masa relativa de un isótopo dado (más específica, cualquier núclido solo), escalado con el carbono-12 como exactamente 12. No hay otros núclidos distintos al carbono-12 que tengan exactamente un número entero de masas en esta escala. Esto es debido a dos factores: la diferente masa de neutrones y protones que actúan para cambiar la masa total en los núclidos con relaciones protón/neutrón distintos al cociente 1:1 del carbono-12; y no se encontrará un número exacto si existe una pérdida/ganancia de masa diferente a la energía de enlace nuclear relativa a la energía de enlace nuclear media del carbono-12. Sin embargo, puesto que cualquier defecto de masa debido a la energía de enlace nuclear es una fracción pequeña (menos del 1%) comparada con la masa de un nucleón (incluso menos comparado con la masa media por nucleón en el carbono-12, que está moderada a fuertemente unido), y dado que los protones y neutrones difieren en masa unos de otros por una fracción pequeña (aproximadamente 0,0014 uma, la práctica de redondear la masa atómica de cualquier núclido dado o isótopo al número entero más cercano, siempre da el número entero simple del conteo total de nucleones. El conteo de neutrones puede ser derivado por sustracción del número atómico.
RADIO ATOMICO
El radio atómico esta definido como la mitad de la distancia entre dos núcleos de dos átomos adyacentes. Diferentes propiedades físicas, densidad, punto de fusión, punto de ebullición, estos están relacionadas con el tamaño de los átomos. Identifica la distancia que existe entre el núcleo y el orbital más externo de un átomo. Por medio del radio atómico, es posible determinar el tamaño del átomo.
PROPIEDADES:
- En un grupo cualquiera, el radio atómico aumenta de arriba a abajo con la cantidad de niveles de energía. Al ser mayor el nivel de energía, el radio atómico es mayor.
- En los períodos, el radio atómico disminuye al aumentar el número atómico (Z), hacia la derecha, debido a la atracción que ejerce el núcleo sobre los electrones de los orbitales más externos, disminuyendo así la distancia entre el núcleo y los electrones.
- El radio atómico puede ser covalente o metálico. La distancia entre núcleos de átomos "vecinos" en una molécula es la suma de sus radios covalentes, mientras que el radio metálico es la mitad de la distancia entre núcleos de átomos "vecinos" en cristales metálicos. Usualmente, por radio atómico se ha de entender radio covalente. Es inversamente proporcional con el átomo
ELECTROAFINIDAD
La afinidad electrónica (AE) o electroafinidad se define como la energía involucrada cuando un átomo gaseoso neutro en su estado fundamental (de mínima energía) captura un electrón y forma un ion mononegativo:
 .
.
Dado que se trata de energía liberada, pues normalmente al insertar un electrón en un átomo predomina la fuerza atractiva del núcleo, que tiene signo negativo. En los casos en los que la energía sea absorbida, cuando ganan las fuerzas de repulsión, tendrán signo positivo; AE se expresa comúnmente en el Sistema Internacional de Unidades, en kJmol-1.
También podemos recurrir al proceso contrario para determinar la primera afinidad electrónica, ya que sería la energía consumida en arrancar un electrón a la especie aniónica mononegativa en estado gaseoso de un determinado elemento; evidentemente la entalpía correspondiente AE tiene signo negativo, salvo para los gases nobles y metales alcalinotérreos. Este proceso equivale al de la energía de ionización de un átomo, por lo que la AE sería por este formalismo la energía de ionización de orden cero.
Esta propiedad nos sirve para prever que elementos generaran con facilidad especies aniónicas estables, aunque no hay que relegar otros factores: tipo de contraicón, estado sólido, ligando-disolución, etc.
| Grupo | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| Periodo | |||||||||||||||||||
| 1 | H -73 | He 21 | |||||||||||||||||
| 2 | Li -60 | Be 19 | B -27 | C -122 | N 7 | O -141 | F -328 | Ne 29 | |||||||||||
| 3 | Na -53 | Mg 19 | Al -43 | Si -134 | P -72 | S -200 | Cl -349 | Ar 35 | |||||||||||
| 4 | K -48 | Ca 10 | Sc -18 | Ti -8 | V -51 | Cr -64 | Mn | Fe -16 | Co -64 | Ni -112 | Cu -118 | Zn 47 | Ga -29 | Ge -116 | As -78 | Se -195 | Br -325 | Kr 39 | |
| 5 | Rb -47 | Sr | Y -30 | Zr -41 | Nb -86 | Mo -72 | Tc -53 | Ru -101 | Rh -110 | Pd -54 | Ag -126 | Cd 32 | In -29 | Sn -116 | Sb -103 | Te -190 | I -295 | Xe 41 | |
| 6 | Cs -45 | Ba | Lu | Hf | Ta -31 | W -79 | Re -14 | Os -106 | Ir -151 | Pt -205 | Au -223 | Hg 61 | Tl -20 | Pb -35 | Bi -91 | Po -183 | At -270 | Rn 41 | |
| 7 | Fr -44 | Ra | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Fl | Uup | Lv | Uus | Uuo | |
POTENCIAL DE IONIZACIÓN
La energía de ionización, potencial de ionización o EI es la energía necesaria para separar un electrón en su estado fundamental de un átomo o de una molécula. La reacción puede expresarse de la siguiente forma:

Siendo 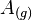 los átomos en estado gaseoso de un determinado elemento químico;
los átomos en estado gaseoso de un determinado elemento químico;  , la energía de ionización y
, la energía de ionización y 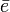 un electrón.
un electrón.
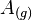 los átomos en estado gaseoso de un determinado elemento químico;
los átomos en estado gaseoso de un determinado elemento químico;  , la energía de ionización y
, la energía de ionización y 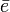 un electrón.
un electrón.
Esta energía corresponde a la primera ionización. El segundo potencial de ionización representa la energía precisa para sustraer el segundo electrón; este segundo potencial de ionización es siempre mayor que el primero, pues el volumen de un ion positivo es menor que el del átomo y la fuerza electrostática atractiva que soporta este segundo electrón es mayor en el ion positivo que en el átomo, ya que se conserva la misma carga nuclear.
El potencial o energía de ionización se expresa en electrón-voltio, Julios o en kilo Julios por mol (kJ/mol).
1 eV = 1,6 × 10-19 C × 1 V = 1,6 × 10-19 J
En los elementos de una misma familia o grupo, el potencial de ionización disminuye a medida que aumenta el número atómico, es decir, de arriba abajo.
Sin embargo, el aumento no es continuo, pues en el caso del berilio y el nitrógeno se obtienen valores más altos que lo que podía esperarse por comparación con los otros elementos del mismo período. Este aumento se debe a la estabilidad que presentan las configuraciones s2 y s2 p3,respectivamente.
La energía de ionización más elevada corresponde a los gases nobles, ya que su configuración electrónica es la más estable, y por tanto habrá que proporcionar más energía para arrancar los electrones.
| Grupo | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| Periodo | |||||||||||||||||||
| 1 | H 1312 | He 2372.3 | |||||||||||||||||
| 2 | Li 520.2 | Be 899.5 | B 800.6 | C 1086.5 | N 1402.3 | O 1313.9 | F 1681.0 | Ne 2080.7 | |||||||||||
| 3 | Na 495.8 | Mg 737.7 | Al 577.5 | Si 786.5 | P 1011.8 | S 999.6 | Cl 1251.2 | Ar 1520.6 | |||||||||||
| 4 | K 418.8 | Ca 589.8 | Sc 633.1 | Ti 658.8 | V 650.9 | Cr 652.9 | Mn 717.3 | Fe 762.5 | Co 760.4 | Ni 737.1 | Cu 745.5 | Zn 906.4 | Ga 578.8 | Ge 762 | As 947.0 | Se 941.0 | Br 1139.9 | Kr 1350.8 | |
| 5 | Rb 403.0 | Sr 549.5 | Y 600 | Zr 640.1 | Nb 652.1 | Mo 684.3 | Tc 702 | Ru 710.2 | Rh 719.7 | Pd 804.4 | Ag 731.0 | Cd 867.8 | In 558.3 | Sn 708.6 | Sb 834 | Te 869.3 | I 1008.4 | Xe 1170.4 | |
| 6 | Cs 375.7 | Ba 502.9 | Lu 523.5 | Hf 658.5 | Ta 761 | W 770 | Re 760 | Os 840 | Ir 880 | Pt 870 | Au 890.1 | Hg 1007.1 | Tl 589.4 | Pb 715.6 | Bi 703 | Po 812.1 | At 920 | Rn 1037 | |
| 7 | Fr 380 | Ra 509.3 | Ac | Ku | Ha | Nt | Gp | Hr | Wl | Mv | Pl | Da | Tf | Eo | Me | Nc | El | On | |
ESTADO DE OXIDACIÓN
En química, el estado de oxidación de un elemento que forma parte de un compuesto u otra especie química, se considera como la carga aparente con la que dicho elemento está funcionando en ese compuesto o especie. Los estados de oxidación pueden ser positivos, negativos, cero, enteros y fraccionarios.
El átomo tiende a obedecer la regla del octeto para así tener una configuración electrónica similar a la de los gases nobles, los cuales son muy estables electricamente. Dicha regla sostiene que un átomo tiende a tener ocho electrones en su nivel de energía más externo. En el caso del hidrógeno este trata de tener 2 electrones, lo cual proporciona la misma configuración electrónica que la del helio.
Cuando un átomo -A- necesita, por ejemplo, 3 electrones para obedecer la regla del octeto, entonces dicho átomo tiene un número de oxidación de 3−. Por otro lado, cuando un átomo -B- tiene los 3 electrones que deben ser cedidos para que el átomo A cumpla la ley del octeto, entonces este átomo tiene un número de oxidación de 3+. En este ejemplo podemos deducir que los átomos A y B pueden unirse para formar un compuesto, y que esto depende de las interacciones entre ellos. La regla del octeto y del dueto pueden ser satisfechas compartiendo átomos (moléculas) o cediendo y adquiriendo electrones (iones poliatómicos).
Los elementos químicos se dividen en 3 grandes grupos, clasificados por el tipo de carga eléctrica que adquieren al participar en una reacción química:
- Metales
- No metales
- Gases nobles
Existen elementos metálicos que, dependiendo de las condiciones a que sean sometidos, pueden funcionar como metales o no metales indistintamente. A estos elementos se les denomina metaloides.
Los elementos metálicos (los cuales ceden electrones) cuando forman compuestos tienen únicamente estados de oxidación positivos. Los elementos no metálicos y semi metálicos pueden tener estado de oxidación positivos y negativos, dependiendo del compuesto que estén constituyendo.
ELECTRONEGATIVIDAD
La electronegatividad, es la medida de la capacidad de un átomo (o de manera menos frecuente un grupo funcional) para atraer hacia él los electrones, cuando forma un enlace químico en una molécula. También debemos considerar la distribución de densidad electrónica alrededor de un átomo determinado frente a otros distintos, tanto en una especie molecular como en sistemas o especies no moleculares. El flúor es el elemento con más electronegatividad, el francio es el elemento con menos electronegatividad.
La electronegatividad de un átomo determinado, esta afectada fundamentalmente por dos magnitudes: su masa atómica y la distancia promedio de los electrones de valencia con respecto al núcleo atómico. Esta propiedad se ha podido correlacionar con otras propiedades atómicas y moleculares. Fue Linus Pauling el investigador que propuso esta magnitud por primera vez en el año 1932, como un desarrollo más de su teoría del enlace de valencia. La electronegatividad no se puede medir experimentalmente de manera directa como, por ejemplo, la energía de ionización, pero se puede determinar de manera indirecta efectuando cálculos a partir de otras propiedades atómicas o moleculares.
| Grupo (Vertical) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| Período (Horizontal) | |||||||||||||||||||
| 1 | H 2,20 | He | |||||||||||||||||
| 2 | Li 0,98 | Be 1,57 | B 2,04 | C 2,55 | N 3,04 | O 3,44 | F 3,98 | Ne | |||||||||||
| 3 | Na 0,93 | Mg 1,31 | Al 1,61 | Si 1,90 | P 2,19 | S 2,57 | Cl 3,16 | Ar | |||||||||||
| 4 | K 0,82 | Ca 1,0 | Sc 1,36 | Ti 1,54 | V 1,63 | Cr 1,66 | Mn 1,55 | Fe 1,83 | Co 1,88 | Ni 1,91 | Cu 1,90 | Zn 1,65 | Ga 1,81 | Ge 2,01 | As 2,18 | Se 2,55 | Br 2,96 | Kr 3,00 | |
| 5 | Rb 0,82 | Sr 0,95 | Y 1,22 | Zr 1,33 | Nb 1,6 | Mo 2,16 | Tc 1,9 | Ru 2,2 | Rh 2,28 | Pd 2,20 | Ag 1,93 | Cd 1,69 | In 1,78 | Sn 1,8 | Sb 2,05 | Te 2,1 | I 2,66 | Xe 2,60 | |
| 6 | Cs 0,79 | Ba 0,89 | * | Hf 1,3 | Ta 1,5 | W 2,36 | Re 1,9 | Os 2,2 | Ir 2,2 | Pt 2,28 | Au 2,54 | Hg 2,00 | Tl 1,62 | Pb 2,33 | Bi 2,02 | Po 2,0 | At 2,2 | Rn 2,2 | |
| 7 | Fr 0,7 | Ra 0,9 | ** | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Fl | Uup | Lv | Uus | Uuo | |
| Lantánidos | * | La 1,1 | Ce 1,12 | Pr 1,13 | Nd 1,14 | Pm 1,13 | Sm 1,17 | Eu 1,2 | Gd 1,2 | Tb 1,1 | Dy 1,22 | Ho 1,23 | Er 1,24 | Tm 1,25 | Yb 1,1 | Lu 1,27 | |||
| Actínidos | ** | Ac 1,1 | Th 1,3 | Pa 1,5 | U 1,38 | Np 1,36 | Pu 1,28 | Am 1,13 | Cm 1,28 | Bk 1,3 | Cf 1,3 | Es 1,3 | Fm 1,3 | Md 1,3 | No 1,3 | Lr 1,3 | |||



No hay comentarios:
Publicar un comentario